【文献精读】阻塞性睡眠呼吸暂停与脑卒中共享生物标志物:WGCNA + 机器学习整合分析
文献信息
PMID: 40540134 IF: 2.0 Q3 | Sleep and Breathing(2025)
标题(英): Exploring the potential biomarkers between stroke and obstructive sleep apnea by WGCNA and machine learning
DOI: 10.1007/s11325-025-03369-1 IF: 2.0 Q3
研究背景
脑卒中(Stroke)与阻塞性睡眠呼吸暂停(OSA)是两大全球公共卫生负担。脑卒中居全球死因第二位,占WHO统计总死亡数的约11%;OSA影响全球近10亿成年人(女性6%-19%,男性13%-33%)。超过50%的脑卒中患者合并OSA,两病共享高血压、糖尿病、肥胖等可改变的危险因素,且存在双向关系:OSA独立增加脑卒中风险,脑卒中后也常出现OSA症状。
间歇性缺氧通过活性氧生成和促炎细胞因子激活促进动脉粥样硬化,可能加重脑缺血。然而,两病共同发生的分子机制尚不清楚。本研究将WGCNA、差异表达分析(DEA)与机器学习相结合,系统识别脑卒中-OSA的共享生物标志物。
材料与方法
数据来源
- 训练集:GSE58294(脑缺血性卒中,69例 vs 23对照)+ GSE135917(OSA,24例 vs 8对照)
- 验证集:GSE22255(脑卒中)+ GSE38792(OSA)
使用SVA包ComBat函数校正批次效应,limma包标准化和协变量调整。
分析流程
- limma包差异表达分析(DEA,P < 0.05)
- WGCNA v1.73共表达网络(|CC| > 0.6,P < 0.05)
- DEGs与WGCNA模块基因交集 → 共享DEGs
- LASSO回归 + 随机森林双重机器学习筛选Hub基因
- ROC曲线评估诊断效力 + GSEA通路分析
研究结果
图1 | 研究流程
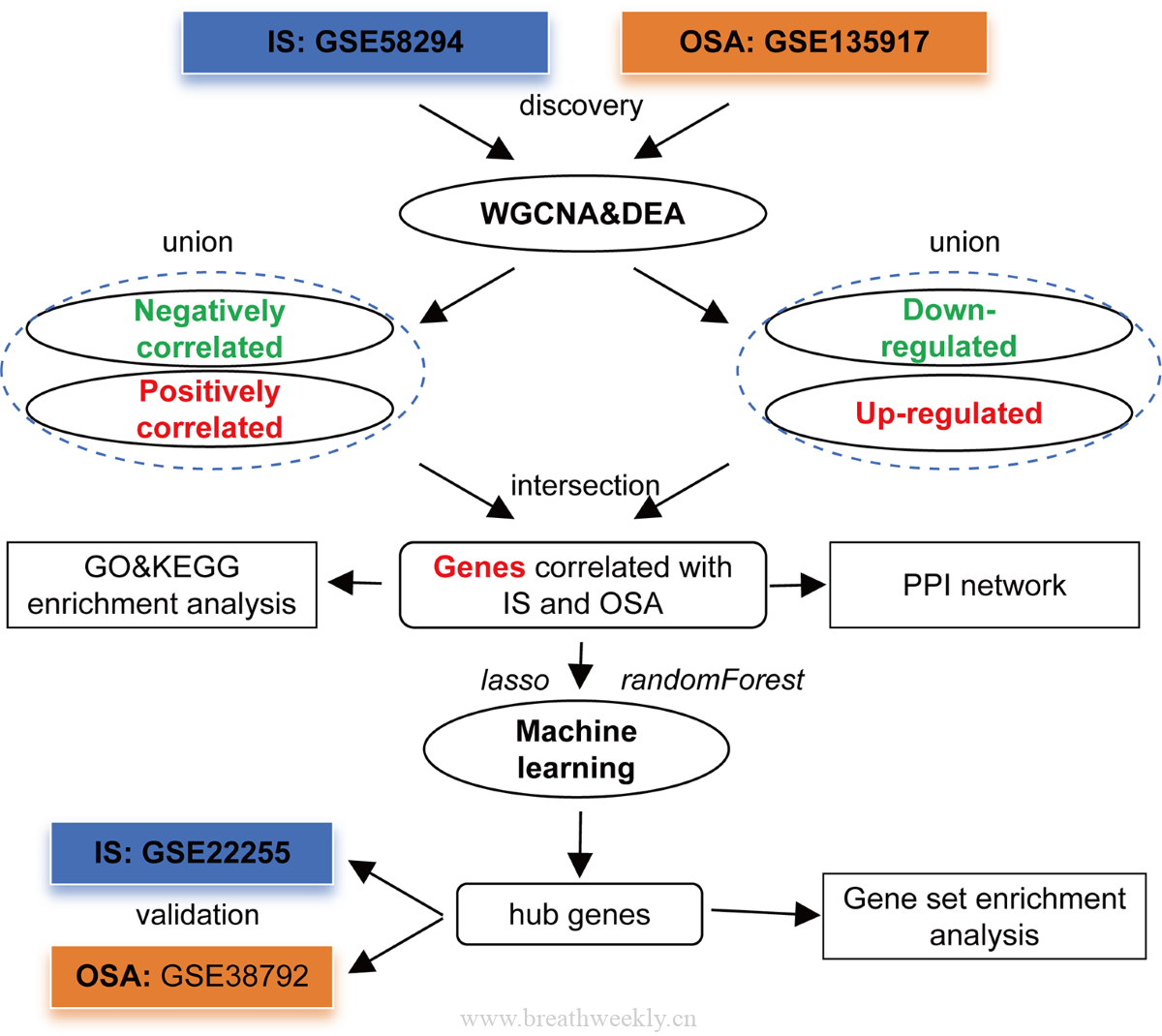
图2 | 批次效应校正
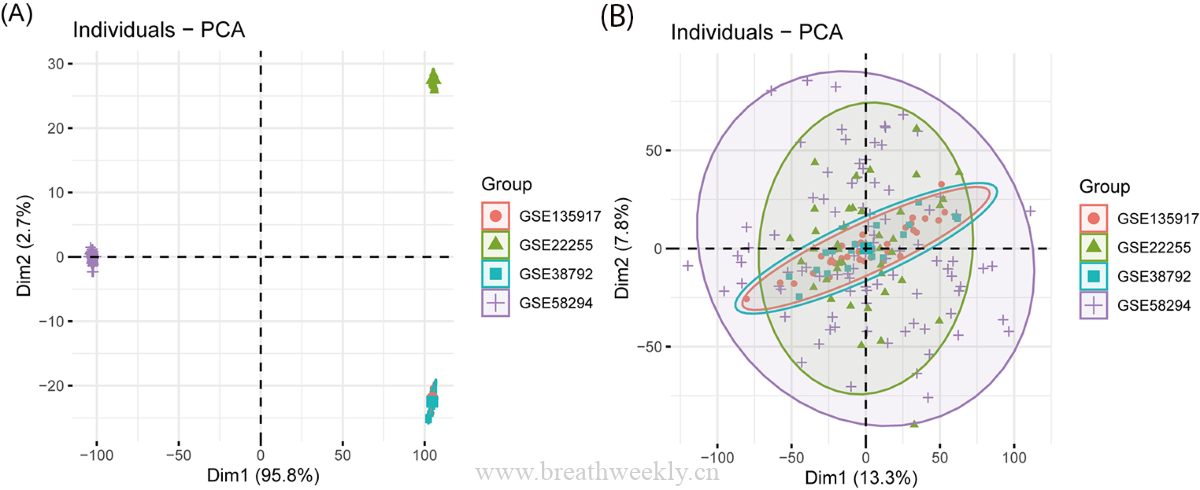
图3 | 差异表达分析
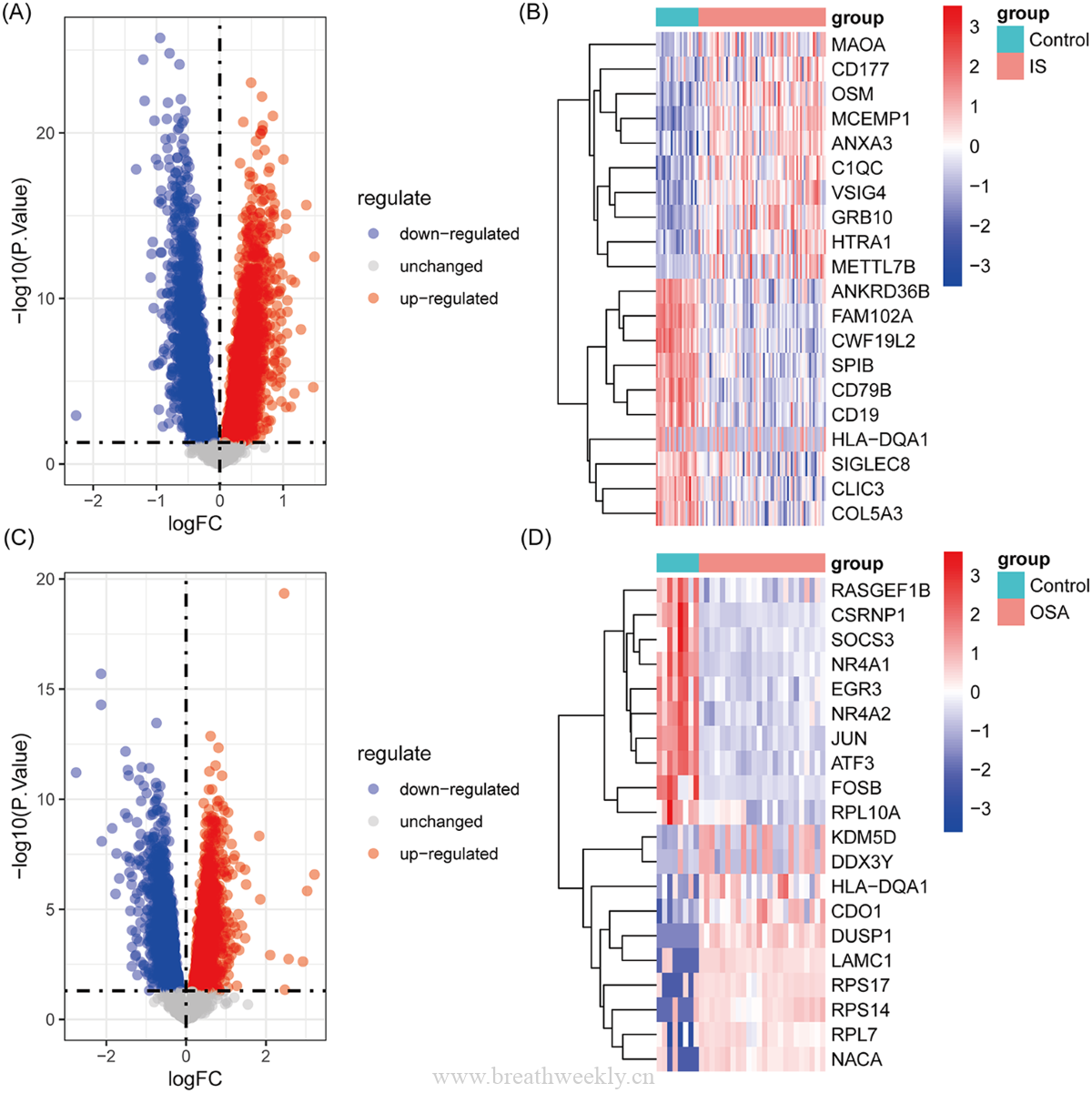
- 脑卒中(GSE58294):2926个上调 + 3175个下调
- OSA(GSE135917):2530个上调 + 2546个下调
图4 | IS数据集WGCNA
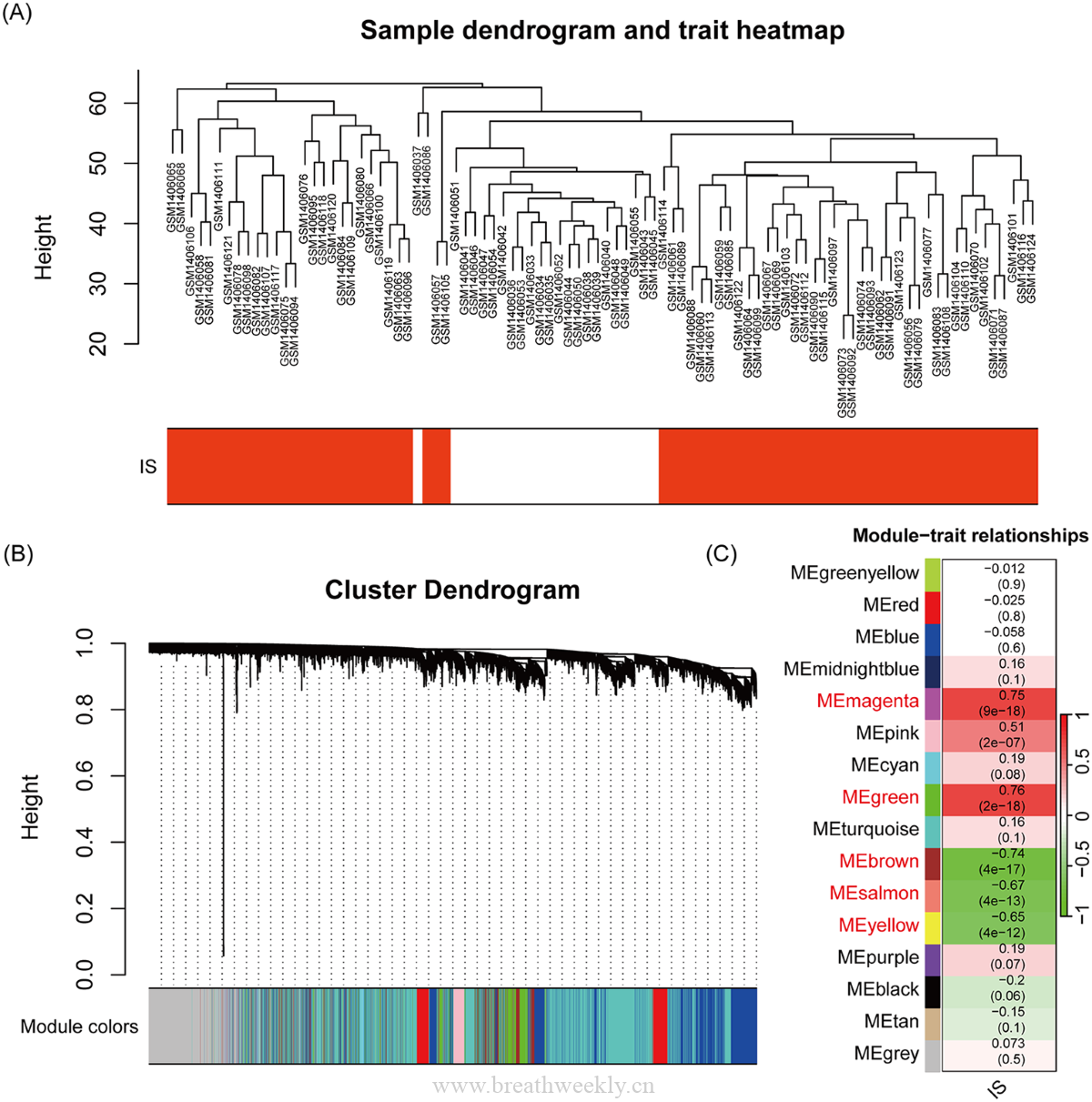
- 16个共表达模块 | 574个基因与IS显著正相关,2403个显著负相关
图5 | OSA数据集WGCNA
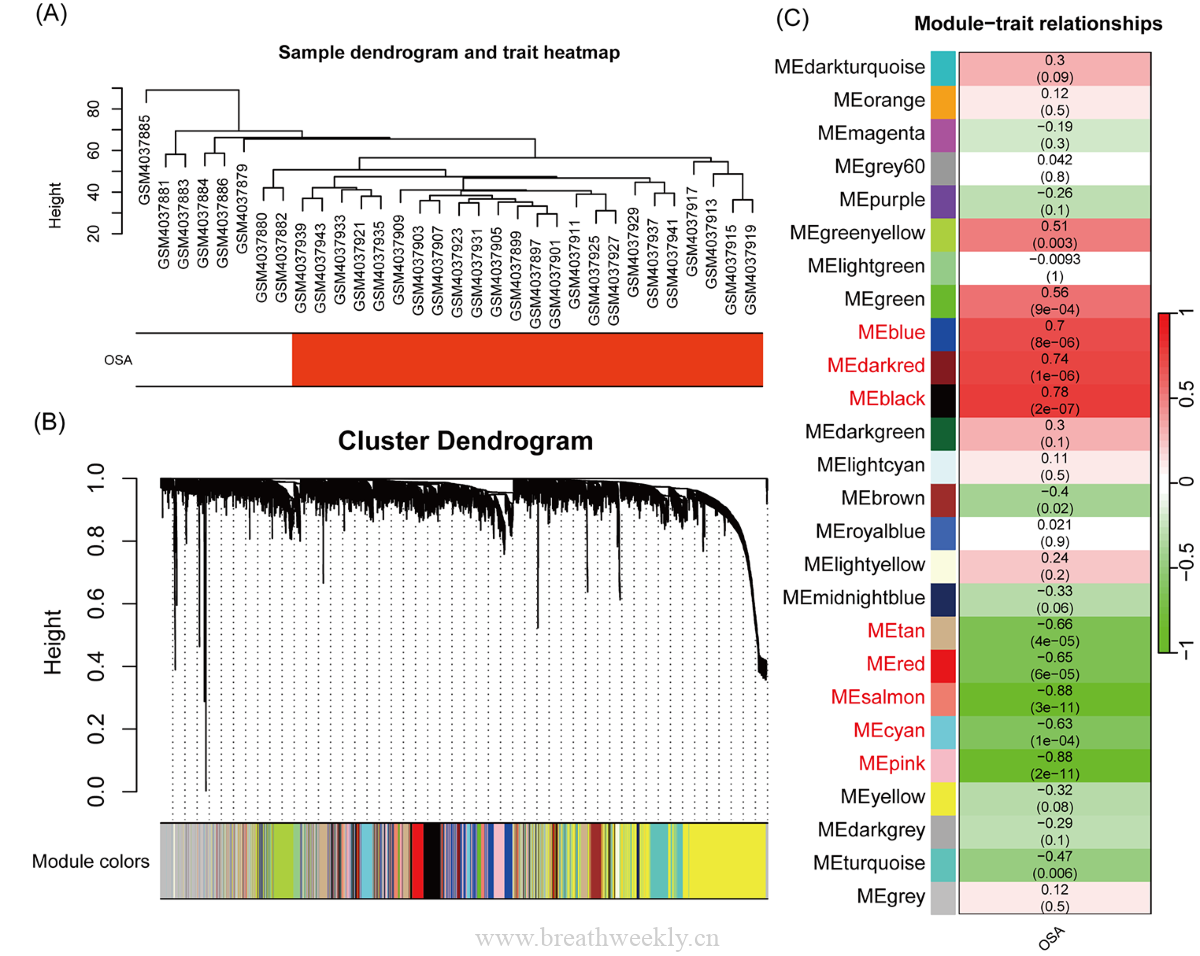
- 26个共表达模块 | 688个基因与OSA显著正相关,1357个显著负相关
图6 | 共享DEGs鉴定
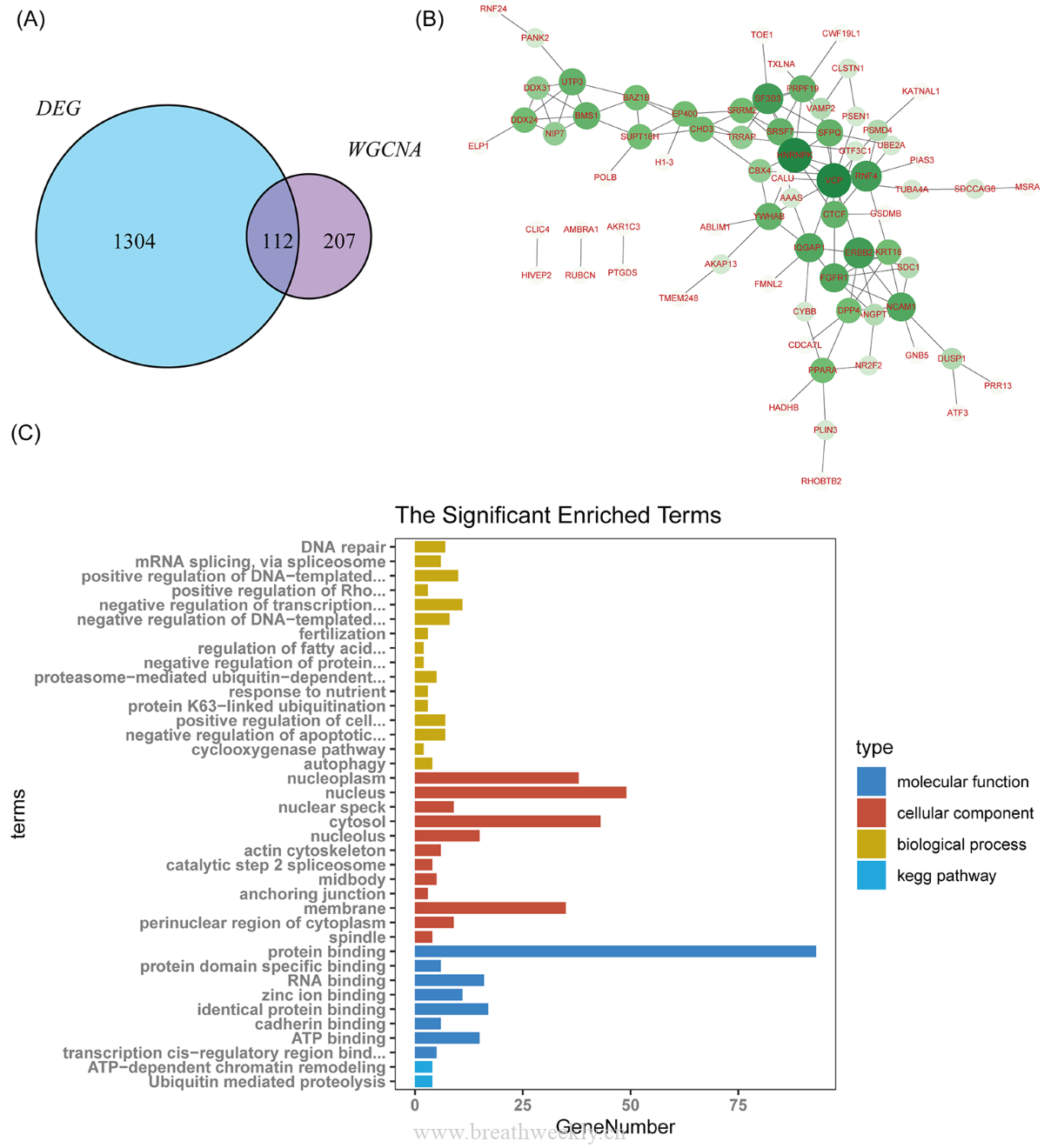
整合DEGs与WGCNA结果,共鉴定出112个共享DEGs(同时与脑卒中和OSA显著相关)。
图7 | DUSP1 Hub基因
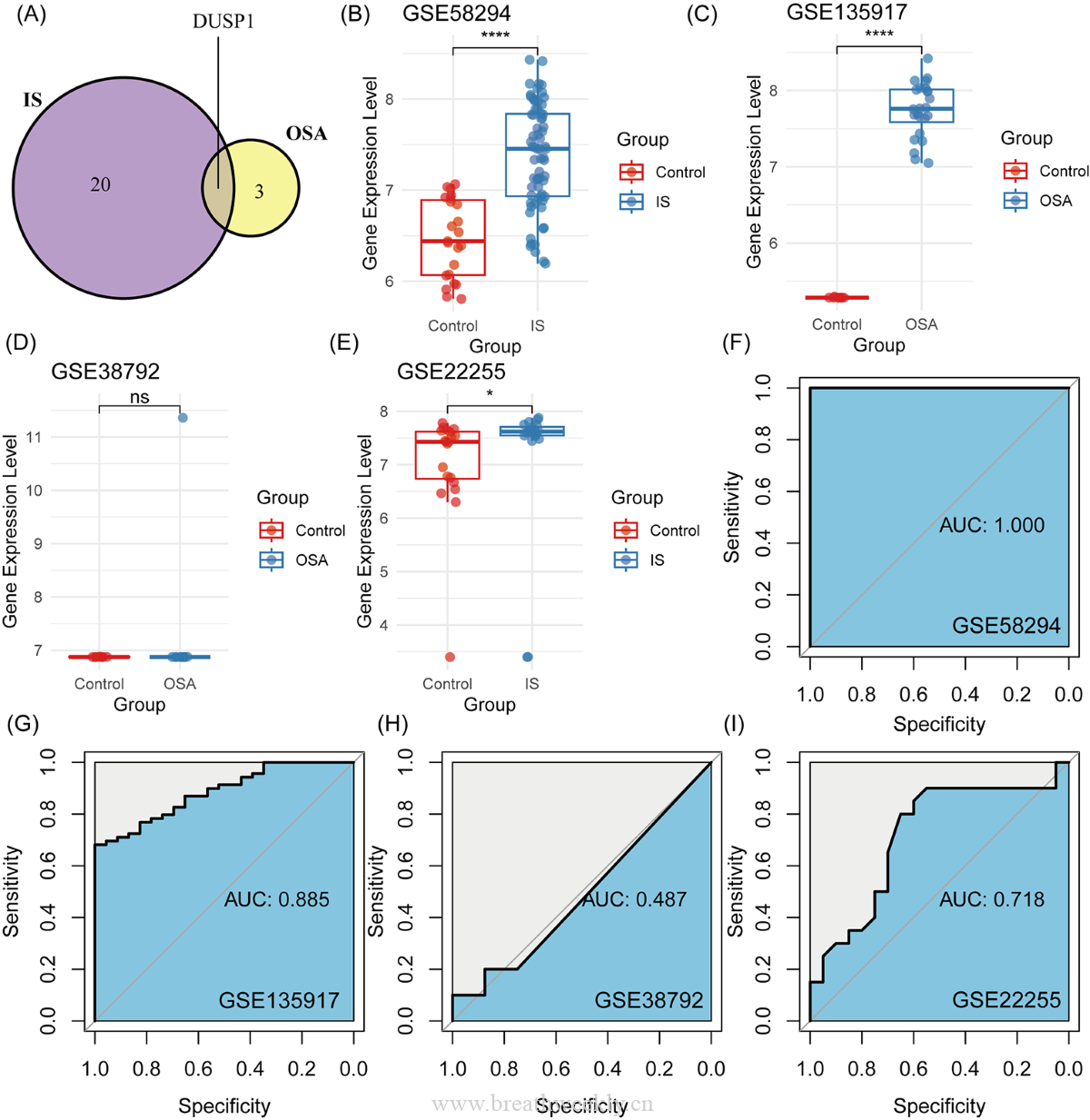
- IS队列:LASSO + RF各筛选15个Hub基因
- OSA队列:LASSO筛选2个,RF筛选4个
- 唯一共有Hub基因:DUSP1(双特异性磷酸酶1)
- DUSP1诊断效能:GSE58294 AUC=1.000 | GSE135917 AUC=0.885 | GSE38792 AUC=0.718 | GSE22255 AUC=0.487
图8 | GSEA机制分析
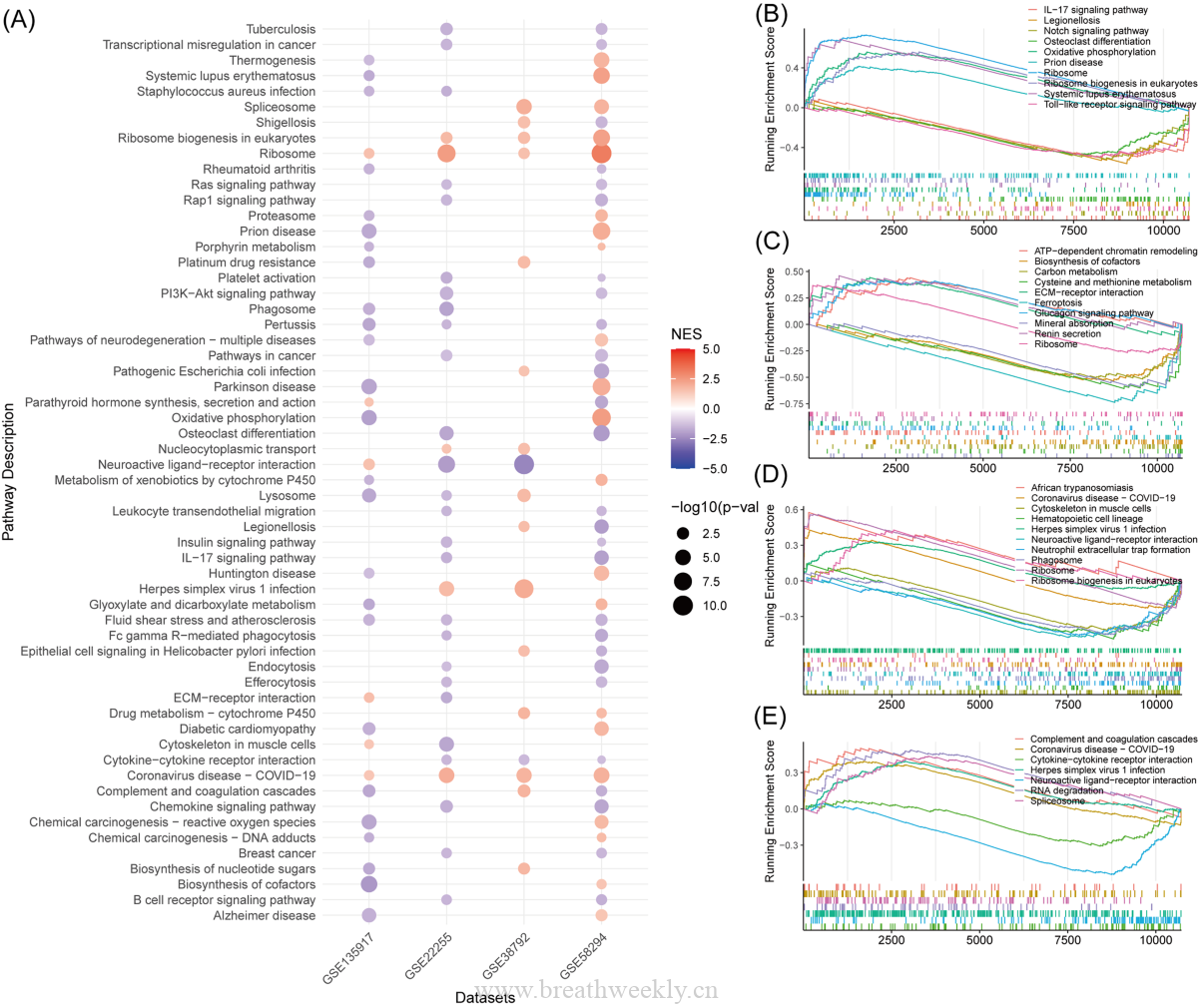
DUSP1高表达组核糖体、剪接体通路激活;Ras/Rap1、PI3K-AKT、IL-17、血小板激活、细胞因子受体相互作用等通路被抑制。58个通路在至少两个队列中显著富集。
讨论
超过50%的脑卒中患者合并OSA。本研究确定了DUSP1作为核心调控基因。GSEA揭示三种共享生物学过程:
- 泛素化:脑卒中中调节CAMKII/PKC/CDK5,OSA中调节PINK1泛素化(FBXL4介导)
- 脂肪酸代谢重编程:脑卒中后小胶质细胞β-氧化上调;OSA中单不饱和脂肪酸和特异性促分解介质与疾病严重程度相关
- 环氧化酶通路:脑卒中中COX通路激活减弱血栓素效应;OSA中LTB4与血压和OSA风险相关
DUSP1作为MAPK(JNK/p38/ERK1/2)的负调节因子,在脑卒中中发挥神经保护作用(抑制JNK、ERK/P38去磷酸化),在OSA中Nr1d1介导的DUSP1抑制增强ERK1/2/DRP1磷酸化,促进线粒体分裂和ROS生成。DUSP1多层保护效应表明它是具有前景的治疗靶点。
研究局限性
- 公开数据集固有变异性可能影响可重复性
- 需蛋白组/代谢组研究全面描述DUSP1的病理作用
- 需体外和体内实验验证DUSP1的具体角色和信号通路相互作用
- OSA-IS共病复杂性提示还有额外Hub基因和通路参与,全面分子图谱仍有待建立
结论
本研究确定DUSP1(双特异性磷酸酶1)为与脑卒中和OSA均显著相关的Hub基因。DUSP1在两种疾病中均高表达并具有强大的诊断效能。与基因表达调控、蛋白泛素化和脂肪酸代谢等生物学过程相关,为两种疾病的潜在分子机制提供了宝贵见解,为开发新的诊断生物标志物和治疗策略奠定了基础。
对OSA课题的借鉴
- GSE135917(OSA)同时被本文和你的课题使用,数据集质量可靠
- 可完全参照WGCNA + LASSO + 随机森林三件套框架
- 加入TwoSampleMR可形成从关联到因果的完整证据链(本文未涉及,是你的创新点)
- DUSP1相关通路(MAPK、PI3K-AKT、IL-17)可纳入富集分析候选列表
- 未来在IH动物模型中验证DUSP1表达具有直接可行性
原文链接:https://doi.org/10.1007/s11325-025-03369-1 IF: 2.0 Q3
所有图片均来自Springer Nature版权文章,仅供学术解读与讨论之用。
Cipher 原创文献解读 | 未经授权禁止转载








暂无评论内容