文献:Jiang F, et al. Identification of shared biomarkers for obstructive sleep apnea and sarcopenia via differential expression and WGCNA analysis. Sleep Breath. 2026.
整理:Roger
更新日期:2026-04-15
标签:阻塞性睡眠呼吸暂停 | 肌少症 | WGCNA | 共享生物标志物 | 生信分析
一、为什么读这篇
这是今年发表的一篇纯生信文章,研究对象是OSA与肌少症的共享生物标志物。之所以选这篇精读,是因为它回答了一个常见疑问:
“纯生信,没有实验验证,什么样的文章才能发表?”
这篇提供了一个可参考的答案。
二、研究背景
临床现象:OSA与肌少症均为增龄相关疾病,临床上常合并出现。OSA患者因夜间低氧和睡眠片段化,可通过炎症通路(NF-κB)、氧化应激、蛋白合成受损等机制促进肌肉消耗;而肌少症导致的肌肉无力又会加重上气道塌陷,形成恶性循环。
科学问题:两病共病的分子机制尚不清晰,是否存在共同的基因表达改变?
研究假设:OSA与肌少症之间存在共享的生物标志物,可作为两病共病的分子桥接证据,同时具备诊断模型开发价值。
三、数据与方法
3.1 数据来源
| 数据集 | 疾病 | 平台 |
|---|---|---|
| GSE135917 | OSA | GEO |
| GSE1428 | 肌少症(Sarcopenia) | GEO |
| GSE38792 | OSA验证集 | GEO |
| GSE111006 | 肌少症验证集 | GEO |
3.2 分析流程
- 差异表达分析(DEGs):分别在两个数据集中筛选疾病组 vs 对照组的差异表达基因
- WGCNA共表达网络分析:构建基因共表达模块,筛选与性状相关的核心模块
- 共享基因交叉定位:取DEGs与WGCNA模块基因的交集(Venn图),得到候选共享基因
- 功能富集分析:GO + KEGG + GSEA,解释候选基因的生物学功能
- 诊断模型构建:基于3个关键基因构建Nomogram诊断模型
- 多维度验证:ROC曲线 + Calibration曲线 + DCA决策曲线 + 外部独立数据集验证
- 免疫浸润分析:CIBERSORT算法分析两组疾病的免疫细胞构成差异
3.3 关键方法参数
| 参数 | 设置 |
|---|---|
| 差异分析FDR校正 | FDR < 0.05,|logFC| > 1 |
| WGCNA soft-threshold | OSA: R2=0.80;肌少症: R2=0.90 |
| 免疫浸润算法 | CIBERSORT |
| 统计方法 | 双样本t检验 + 双侧ANOVA(Tukey post hoc) |
四、主要结果
4.1 差异表达与共享基因
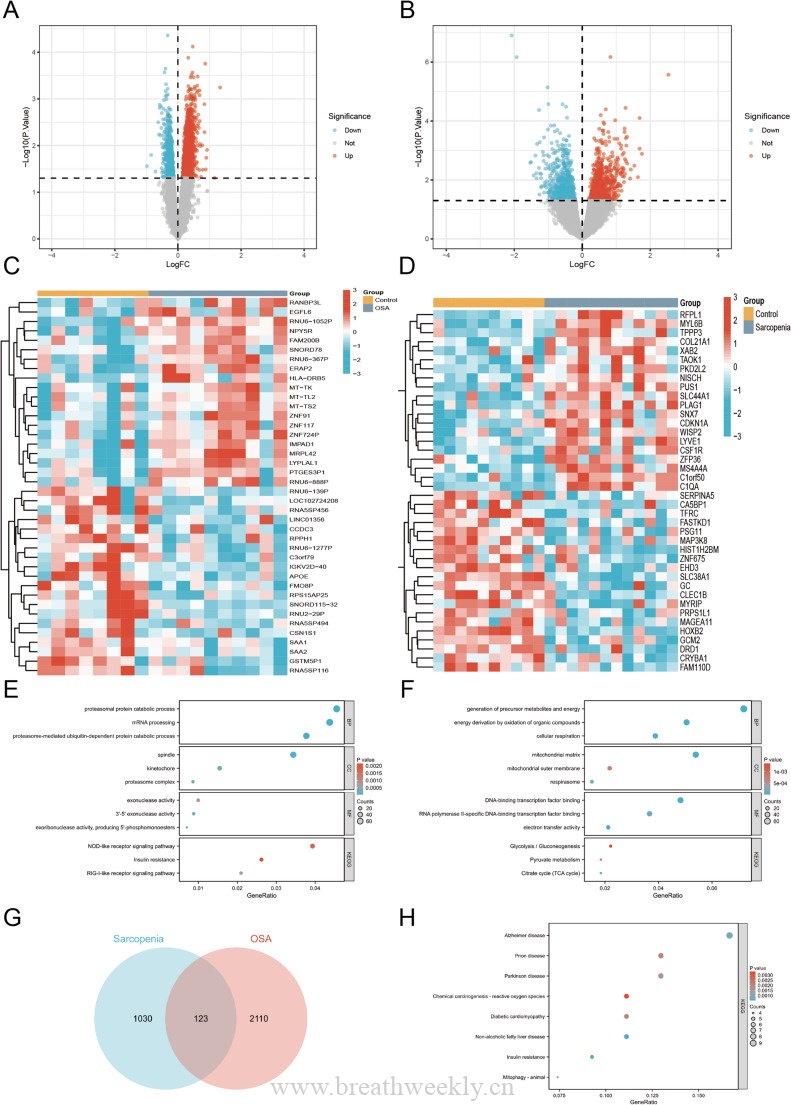
在两个数据集中分别筛选出差异表达基因后,取交集得到123个共享DEGs。这些基因富集于肌肉功能、细胞应激、代谢紊乱和神经退行性相关通路。

图2. 差异基因筛选火山图、热图及富集分析结果。(A-B)GSE135917和GSE1428的DEGs火山图;(C-D)热图;(E-F)GO和KEGG富集分析;(G)123个共享DEGs的Venn图;(H)共享DEGs的KEGG通路分析。
4.2 WGCNA模块分析
通过WGCNA构建共表达网络,鉴定出与OSA和肌少症性状高度相关的核心模块,进一步与DEGs交叉定位,得到9个高度可信的共享候选基因。该步骤的关键结果包括:
- 软阈值筛选:OSA数据集选取R2=0.80对应的power值;肌少症数据集选取R2=0.90
- 模块-性状相关性热图显示多个模块与疾病状态显著相关
- Venn图定位9个同时存在于两个疾病WGCNA模块中的共享基因
图3
4.3 关键共享生物标志物
经过DEGs + WGCNA双重筛选,最终锁定3个核心基因:
| 基因 | 功能注释 |
|---|---|
| ESF1 | 进化保守的核蛋白,参与核糖体生物合成和细胞增殖调控 |
| ZNF117 | 锌指蛋白,参与转录调控和蛋白质相互作用 |
| C2orf49 | 2号染色体开放阅读框,功能尚未完全阐明 |

图5. 三个关键基因的表达量与诊断价值评估。(A-C)ESF1、ZNF117、C2orf49在训练集的表达;(D-F)验证集的表达;(G-I)各基因ROC曲线;(N-O)Nomogram模型在两个数据集的ROC表现。
4.4 诊断模型表现
| 数据集 | 疾病 | 训练集 AUC | 验证集 AUC |
|---|---|---|---|
| GSE135917 / GSE38792 | OSA | 0.912 | 0.787 |
| GSE1428 / GSE111006 | 肌少症 | 0.967 | 0.744 |
4.5 免疫浸润分析
CIBERSORT分析显示,OSA和肌少症组中促炎免疫细胞(如M1巨噬细胞、活化NK细胞)比例均显著升高,且关键基因表达与促炎细胞浸润呈正相关,提示免疫炎症是两病共享的病理基础。

图7. 两组疾病的免疫细胞构成分析及与关键基因的相关性。(A-C)OSA组免疫细胞构成;(D-F)肌少症组免疫细胞构成;(C、F)关键基因与免疫细胞的相关性热图。
五、为什么这篇纯生信能发表?
5.1 临床假设创新性强
不是单纯的”OSA生信分析”,而是跨疾病的共享生物标志物研究——这是两种在临床上确实存在共病的疾病,机制上有合理的病理生理关联假设。
5.2 分析链条完整,没有明显短板
DEGs + WGCNA + 功能富集 + 诊断模型 + 多维度验证 + 免疫浸润,每一步都有且衔接紧密。
5.3 外部独立验证是硬通货
有独立的验证数据集(GSE38792、GSE111006),且验证集AUC仍在0.74-0.79区间——双疾病、双验证集的配置显著提升了结论可信度。
5.4 诊断模型+DCA增加了临床转化价值
不仅找了基因,还构建了Nomogram并做了DCA决策曲线——这让文章从”机制探索”升级为”临床工具开发”。
5.5 期刊选择精准
发表在Sleep Breath(ESCI),专业对口接收这类”睡眠疾病+生信”的研究。
六、值得借鉴的方法与思路
6.1 分析框架可以直接迁移
对于OSA认知障碍方向,研究逻辑完全可以套用:
OSA数据集(GEO) + 认知障碍数据集(GEO) → DEGs分析 → WGCNA共表达网络 → 与TRPM2/CREB/BDNF通路基因交叉定位 → 构建诊断模型 → 外部验证 → 免疫浸润分析
6.2 “双重筛选”策略值得学习
DEGs + WGCNA模块基因取交集,比单纯DEGs更有生物学意义——筛选出的基因在共表达网络中本身就有关系,不只是统计显著。
6.3 免疫浸润是加分项
CIBERSORT分析已经是纯生信的”标配加分项”,且这篇文章将其与关键基因表达做了相关性分析,形成了从基因到免疫微环境的完整叙事。
6.4 Nomogram + DCA是可视化亮点
Nomogram对于临床医生读者非常直观,DCA则量化了模型的临床净获益。这两个图在投稿时能给reviewer留下深刻印象。
6.5 对Roger课题的直接启发
姜黄素改善OSA认知障碍的研究,完全可以在GEO上做:
- 用认知障碍数据集(如阿尔茨海默病、认知损害相关数据集)作为认知障碍对照
- 与OSA数据集取交集
- 关注TRPM2/CREB/BDNF通路的基因表达变化
- 用姜黄素处理IH细胞或动物的RNA-seq数据做进一步验证
这样生信是”上游筛选”,动物实验是”下游验证”,逻辑链条完整。
七、参考文献
- Jiang F, et al. Identification of shared biomarkers for obstructive sleep apnea and sarcopenia via differential expression and WGCNA analysis. Sleep Breath. 2026. PMID: 41784837 IF: 2.0 Q3 .
- Gozal D, et al. Cognitive dysfunction and metabolic alterations in rats with chronic intermittent hypoxia. Am J Respir Crit Care Med. 2003.
- Gold PE, et al. Behavioral and molecular responses to intermittent hypoxia. Am J Respir Crit Care Med. 2003.
本文为文献周报,如有解读不当之处,欢迎交流指正。







暂无评论内容