作者:田博(Roger)
发布日期:2026-05-13
标签:阻塞性睡眠呼吸暂停 | CXCR4 | 心血管风险 | 干细胞归巢 | CPAP不可逆
引言:CPAP治不好心血管风险的谜题
阻塞性睡眠呼吸暂停(OSA)是心血管疾病(心梗、脑梗、房颤、心衰)的独立危险因素。然而,多项大型RCT(SAVE、RICCADSA等)一致显示:CPAP治疗不能显著降低OSA患者的心血管事件风险。这一临床悖论提示,OSA对心血管系统的损害存在某种不可逆成分——CPAP消除了间歇低氧,但未能修复更底层的分子缺陷。
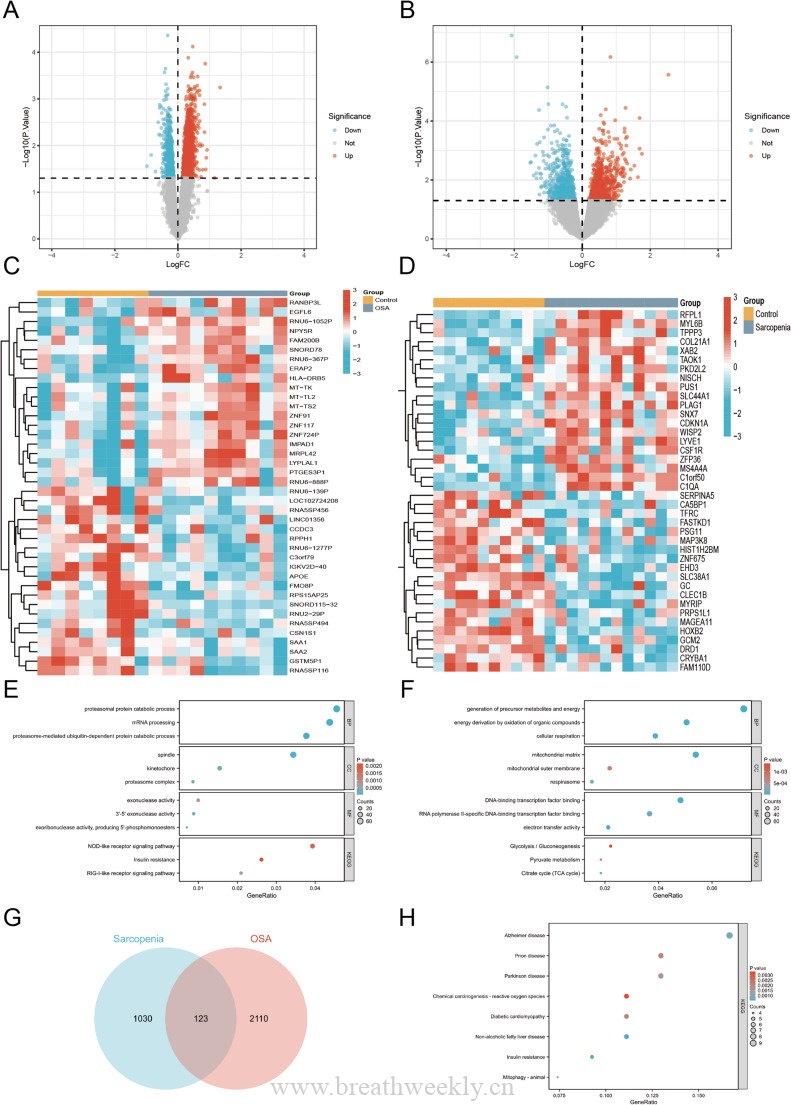
我们对GSE283703数据集(71例PBMC RNA-seq)的系统分析发现,CXCR4是47个CPAP不可逆基因中唯一与所有4种主要心血管共病共享的差异基因。这一发现为”CPAP不能消除心血管风险”提供了分子层面的解释。
CXCR4的正常功能:干细胞的GPS导航系统
CXCR4是表达在免疫细胞和造血干细胞表面的趋化因子受体,其配体SDF-1(CXCL12)主要由骨髓基质细胞和损伤组织分泌。
正常状态下,CXCR4-SDF-1轴执行两大关键功能:
- 骨髓锚定:骨髓基质持续分泌SDF-1 → 形成浓度梯度 → 干细胞表面CXCR4感知梯度 → 干细胞”锚定”在骨髓微环境中 → 维持干细胞池
- 损伤归巢:组织损伤(如心梗)→ 损伤部位释放SDF-1 → 表达CXCR4的干细胞沿SDF-1梯度迁移 → 归巢到损伤部位 → 参与组织修复
简单说,CXCR4 = 干细胞的GPS导航系统,SDF-1 = 目的地发出的信号。没有CXCR4,干细胞找不到该去的地方。
OSA导致CXCR4不可逆下调的后果
我们的数据显示,OSA患者PBMC中CXCR4显著下调,且CPAP治疗24个月后仍不可逆。这意味着:
后果1:干细胞归巢到损伤部位的能力下降
心梗发生 → 心肌释放SDF-1 → 发出”求救信号” → 但OSA患者PBMC上CXCR4表达低 → 干细胞”接收不到信号” → 归巢到心肌的细胞减少 → 心肌修复不足 → 梗死面积更大 → 预后更差
后果2:免疫监视能力下降
CXCR4下调 → T细胞、NK细胞迁移到炎症部位的能力减弱 → 慢性低度炎症持续 → 血管内皮损伤加速 → 动脉粥样硬化进展
后果3:造血干细胞”无效循环”
CXCR4低表达 → 干细胞与骨髓基质”粘不住” → 过早泄漏到外周血 → 但因CXCR4低,又无法有效归巢到需要修复的组织 → 外周血干细胞数量可能正常甚至升高,但功能是”无效的”——在血液里飘着,到不了该去的地方
为什么CPAP治不好CXCR4
CPAP消除了间歇低氧和睡眠片段化,但CXCR4仍下调。可能原因:
- 表观遗传记忆:间歇低氧通过DNA甲基化或组蛋白修饰沉默了CXCR4启动子,这些修饰在CPAP后不自动逆转
- 上游转录因子持续抑制:我们的TF分析显示USF1/USF2是CXCR4的上游调控因子,如果USF通路本身也受不可逆影响,CXCR4就无法恢复
- 骨髓微环境重塑:长期间歇低氧可能改变了骨髓基质细胞分泌SDF-1的模式,形成新的稳态,CPAP纠正了外周氧供但没纠正骨髓微环境
AMD3100(Plerixafor):看似矛盾的补偿策略
这看起来矛盾——CXCR4已经低了,为什么还要用拮抗剂进一步阻断?关键在于理解AMD3100的作用机制不同于简单的”抑制”。
正常骨髓
骨髓基质 ──SDF-1──→ CXCR4(干细胞) → 干细胞”锚定”在骨髓
AMD3100的作用
AMD3100竞争性结合CXCR4 → 阻断SDF-1-CXCR4结合 → 干细胞从骨髓”脱锚” → 释放到外周血
OSA患者的问题
骨髓:SDF-1正常分泌,但干细胞CXCR4低 → 部分干细胞已经”锚不牢” → 泄漏到外周血
外周血:干细胞CXCR4低 → 无法归巢到损伤部位 → “无效循环”
AMD3100的补偿逻辑
- AMD3100把骨髓里CXCR4表达尚可的干细胞也动员出来 → 大幅增加外周血干细胞数量
- 虽然这些细胞CXCR4表达偏低,但数量补偿质量——更多干细胞在循环中,即使归巢效率低,总归巢数仍可能增加
- 更重要的是,AMD3100是短暂给药(皮下注射后数小时起效),停药后CXCR4功能恢复 → 此时干细胞已经在外周血中 → 可以响应损伤部位的SDF-1信号
类比:OSA患者的情况 = 城市里出租车GPS坏了,车在路上跑但找不到乘客。AMD3100 = 先把所有出租车从车库放出来(数量大增),然后GPS短暂恢复(停药后CXCR4解离),出租车就能接客了。
临床证据
- 心梗:AMD3100在心梗动物模型中改善心肌修复(Penn MS 2012, PMID: 22797961;Jujo K 2013, PMID: 23636719)
- 脑梗:AMD3100促进神经干细胞动员和功能恢复(Shen Q 2019, PMID: 31451703)
- 已批准:Plerixafor(AMD3100商品名)2008年获FDA批准用于非霍奇金淋巴瘤和多发性骨髓瘤的干细胞动员,安全性已有临床数据
写在最后
CXCR4的不可逆下调可能是OSA患者心血管事件预后差的分子基础。这一发现将”CPAP不能消除心血管风险”这一临床难题,从现象层面推进到了机制层面。而CXCR4通路调控(如AMD3100动员干细胞)可能是一种补偿性治疗策略——不是修复CXCR4本身,而是绕过它的缺陷,用数量优势弥补归巢效率的不足。
当然,这仍是基于生信分析的假说,需要间歇低氧动物模型和心血管损伤模型的实验验证。
本文基于GSE283703数据集的转录组分析结果,详见:田博等,”Transcriptomic mapping of CPAP-irreversible genes and circadian disruption in obstructive sleep apnea”(投稿中)






暂无评论内容